阿尔茨海默病(AD)是一种神经退行性疾病,好发于老年人群体,确切的AD发生机制仍然不明。现有批准的AD治疗方法主要针对当前患者的神经病理学,疗法的有效性不佳。由于缺乏检测人类大脑中疾病进展的非侵入性技术,研究人员往往依赖于AD模型用以跟踪疾病的产生、影响大脑的方式以及探寻潜在的治疗策略。能否密切反应阿尔茨海默病在现实生活中的进展方式是体现模型价值的重要依据。
近日,研究人员展示了一种基于诱导多能干细胞(iPSC)构建的阿尔茨海默病模型,或有助于加深AD在大脑中进展的理解。
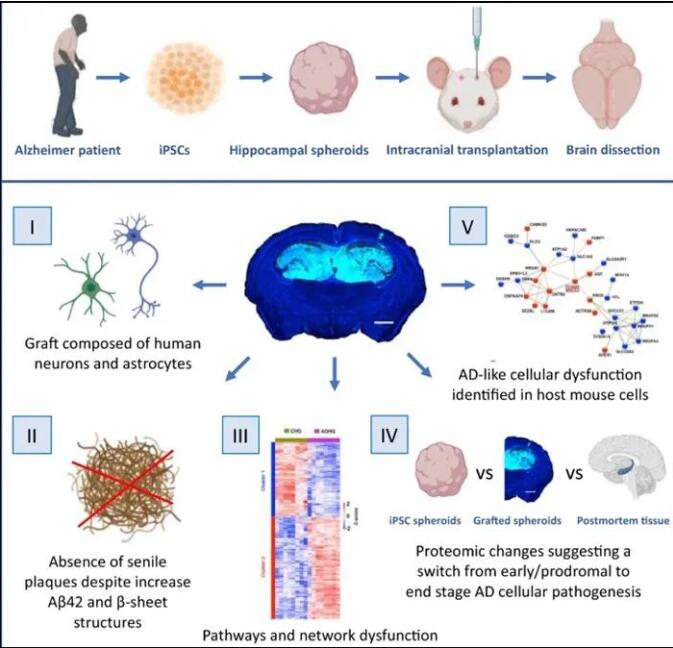
研究人员利用iPSC诱导形成包括神经元等大脑相关细胞类型,从而允许他们可以研究与患者具有相同遗传背景的人类脑细胞。随后研究人员将AD患者iPSC衍生脑细胞移植到免疫缺陷的野生型小鼠大脑中,为产生的脑细胞构建了一个受到严格调节的能促进细胞健康和功能的大脑微环境。
基于这种大脑模型,研究人员检测了包括蛋白斑块和缠结物、炎症、线粒体功能障碍、病变迁移能力等AD特征性病变进展情况,更好反映实际的疾病过程。结果发现,该模型成功再现大脑通路中可能导致淀粉样蛋白斑块形成的关键变化,以及邻近脑细胞中与疾病的相关变化,可能是疾病在细胞间扩散的迹象;通过蛋白质组分析,他们还揭示疾病从早期进展到晚期的全部变化。
综上,该研究构建了一种贴近AD患者大脑的嵌合模型,或有助于更好理解AD在大脑中的进展,进而开发更为有效的早期筛查和治疗策略。

