肝纤维化的特征是过度瘢痕化,这是由各种肝病(如饮酒、非酒精性脂肪性肝炎(NASH)和丙肝(HCV)感染)引发的慢性炎症过程引起的。肝纤维化是慢性肝病进展中不可分割的一部分,最终导致肝硬化和HCC。炎症、组织修复和细胞外基质沉积相关通路的损伤可导致肝纤维化的发展。
microrna (miRs)是一种小的调节rna,在肝脏疾病中经常被解除调控。肝纤维化的特征是由慢性炎症过程引起的过度瘢痕形成。在研究中,通过锁定核酸(LNA)抗mir的方法确定了miR-132在肝纤维化中的功能作用。在CCl4治疗的小鼠和纤维化/肝硬化患者中发现了miR-132水平的显著诱导。在lna -抗miR-132小鼠中,抑制miR-132可降低ccl4诱导的纤维化和炎症表型。
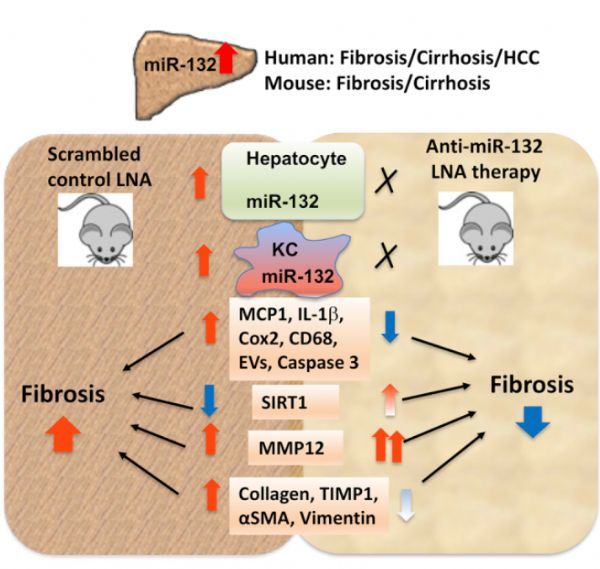
在LNA-anti-miR-132处理的小鼠中发现胶原纤维、SMA、MCP1、IL-1b和Cox2的衰减。CCl4处理组caspase 3活性和细胞外囊泡(ev)增加,而mir - 132处理组小鼠则没有。在肝脏和Kupffer细胞中,miR-132的抑制与MMP12的增加有关。体内和体外研究表明,miR-132靶向SIRT1和炎症基因。
microrna (miRs)是一类小型非编码rna,已成为细胞过程中新的重要调控因子。11 miR-132在大脑中被广泛研究,在多种神经系统疾病中均发现其失调。最近的研究表明miR-132在胃肠道肿瘤的发病机制中发挥作用。几种miRs被证明参与了肝纤维化,然而,到目前为止,只有少数miRs在肝脏疾病中的功能作用被揭示。因此,研究其他miRs的功能丧失和获得是必要的,以进一步了解mir依赖调节肝功能和稳态的机制。然而miR- 132在许多染色质重塑因子参与乙酰化、去乙酰化和氧化应激的调控方面是独特的。
由于慢性酒精滥用导致肝纤维化/肝硬化,假设miR-132在这一过程中发挥了致病作用。与该假设一致,发现酒精性纤维化/肝硬化患者的肝脏中有4倍的miR-132诱导。在用CCl4治疗的小鼠肝脏中发现了显著的miR-132的诱导,CCl4是一种建立已久的肝纤维化诱导物。小鼠给予LNA(锁定核酸)- anti-miR-132后,发现ccl4诱导的肝纤维化减弱。
