研究发现EFNA4基因敲除可抑制肝癌细胞的增殖和迁移
作者:互联网
日期:2021-09-16
肝癌是最常见的恶性肿瘤之一,2018年全球男性死亡率居第四位,癌症相关死亡率居第二位。大多数肝癌患者在确诊时已进入疾病的晚期,对于那些错过手术机会的患者来说,分子靶向治疗变得更加重要。
快速的肿瘤进展、转移和晚期诊断是肝癌患者生存时间短、死亡率高的主要原因。肾上腺素A4(EFNA4)是促肾上腺皮质激素(EPH)家族的配体,通过调节细胞迁移和排斥反应参与血管和上皮的发育。
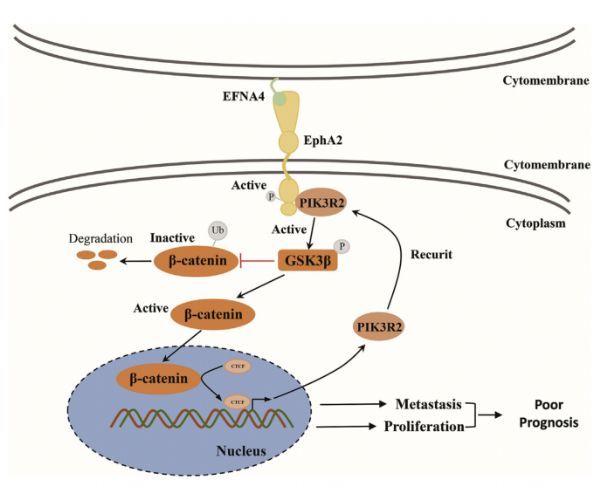
在该研究中,基于生物信息学的分析,研究者发现EFNA4在肝癌患者中高表达并导致预后不良。此外,EFNA4基因敲除可抑制肝癌细胞的增殖和迁移。此外,还发现EFNA4直接与EphA2相互作用并促进其在Ser897处的磷酸化,然后是磷脂酰肌醇-3-激酶调节亚单位2(PIK3R2)的募集和糖原合成酶激酶-3β(GSK3b)/b-catenin信号通路的激活。结果表明,EFNA4的异常表达是PIK3R2/GSK3b/b-catenin环的主要开关,影响肝癌细胞的增殖和迁移,提示EFNA4是肝癌患者潜在的预后标志物和潜在的治疗靶点。
虽然酪氨酸激酶抑制剂(TKIs)是晚期肝癌患者的一线治疗药物,但TKIs(如索拉非尼)容易产生耐药性。因此,索拉非尼增强剂或抗体-药物偶联物(ADCs)等肝癌新治疗方案的发现已成为肝癌临床治疗的迫切需要。
促肾上腺皮质激素/肾上腺素(EPH/EFN)系统通过与细胞膜结合,在多种细胞中广泛表达。它在细胞的发育、增殖和分化过程中起着至关重要的作用,它通过细胞与细胞的接触、细胞信号的调节和向细胞核的转移以及下游信号通路的刺激等与肿瘤的发生密切相关。此外,根据基因序列同源性、结构域和亲和力的差异,有9种类型的EPHA受体和5种类型的EPHB受体。
EPH受体相互作用蛋白(EFN配体)分为8个亚型,即5个EFNA配体和3个EFNB配体。当受体与相邻细胞的配体结合时,聚合物就会形成,双向信号就会激活。EFNA配体与相应的EPH受体结合,通过改变EPH的构象激活受体细胞质中的酪氨酸激酶,导致相应受体的磷酸化和下游信号的激活。此外,efna配体激活宿主细胞的相关表面受体,如p75nt受体(P75ntr)。
EFNA4主要在成人的脾、淋巴结、卵巢、小肠和结肠中表达,在胎儿的心、肺、肝和肾中也有表达。它通过调节细胞迁移、排斥和粘附参与神经元、血管和上皮的发育。研究表明,EFNA4与胶质瘤、卵巢癌、慢性淋巴细胞白血病等肿瘤的增殖和转移有关。
基于公共数据库分析(癌症基因组图谱[TCGA]和基因表达总览[GEO]),作者发现EFNA4在HCC中高表达,且与较差的疾病预后相关。EFNA4的表达增加促进HCC细胞的增殖和迁移能力。从机制上讲,EFNA4的过表达激活了Ser897上EphA2受体的磷酸化。随后,磷脂酰肌醇-3-激酶调节亚单位2(PIK3R2)/糖原合成酶激酶-3β(GSK3b)/b-catenin轴影响肝癌细胞的增殖和迁移。因此,这些发现提示EFNA4可以作为一个预后标志物,靶向EFNA4可能是晚期肝癌患者的一种潜在的治疗策略。


